Описание препарата Тилкотил® (суппозитории ректальные, 20 мг) основано на официальной инструкции, утверждено компанией-производителем в 2000 году
Дата согласования: 31.07.2000
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав и форма выпускa
- Фармакологическое действие
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Меры предосторожности
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Тилкотил®
Действующее вещество
ATX
Фармакологическая группа
Состав и форма выпускa
1 таблетка, покрытая оболочкой, содержит теноксикама 20 мг; в коробке 3 блистера по 10 шт.
1 ректальный суппозиторий — 20 мг; в блистере 5 шт., в коробке 2 блистера.
Фармакологическое действие
Ингибирует синтез ПГ (угнетает активность циклооксигеназы 1 и циклооксигеназы 2), снижает накопление лейкоцитов в очаге воспаления.
Ингибирует синтез ПГ (угнетает активность циклооксигеназы 1 и циклооксигеназы 2), снижает накопление лейкоцитов в очаге воспаления.
Фармакодинамика
Оказывает мощное и длительное болеутоляющее (наступает через 30 мин) и противовоспалительное действие при менее выраженном жаропонижающем. При ревматических заболеваниях ослабляет боль в суставах в покое и при движении, уменьшает утреннюю скованность и припухлость, улучшает функции и увеличивает объем движений суставов.
Фармакокинетика
Быстро и полно всасывается в ЖКТ. Биодоступность 100%. Cmax достигается через 2 ч. Связывается с белками плазмы на 99%. Объем распределения — 0,15 л/кг. T1/2 — 60–75 ч. В печени гидроксилируется. Легко проходит гистогематические барьеры. Основная часть выводится в виде неактивных метаболитов с мочой, остальная — с желчью.
Показания
Воспалительно-дегенеративные заболевания опорно-двигательного аппарата, сопровождающиеся болевым синдромом: суставной синдром при подагре, ревматоидный артрит, остеоартроз, анкилозирующий спондилоартрит, остеохондроз, суставной ревматизм (тендиниты, бурситы, миозиты), боли в позвоночнике, невралгии, миалгии, травмы.
Противопоказания
Гиперчувствительность, активная пептическая язва, выраженные нарушения функции печени в активной стадии, почечная недостаточность, сахарный диабет, артериальная гипертензия, сердечная недостаточность, детский возраст.
Применение при беременности и кормлении грудью
Противопоказано.
Способ применения и дозы
Внутрь, ректально. По 1 табл. или 1 супп. 1 раз в день (желательно в одно и то же время).
При острых приступах подагры по 2 табл. или 2 супп. 1 раз в сутки в течение первых двух дней, затем по 1 табл. или 1 супп. 1 раз в день в течение 5 дней.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Тошнота, изжога, боли в животе, диарея, метеоризм, стоматит, анорексия, эрозивно-язвенные поражения, кровотечения, головная боль, головокружение, бессонница, депрессия, повышенная возбудимость, отек в области глаз, раздражение глаз, нарушение зрения, периферические отеки, повышение концентрации в плазме креатинина, мочевины азота, билирубина и активности печеночных трансаминаз, аллергические реакции (крапивница, зуд); при применении суппозиториев возможно местное раздражение, болезненная дефекация.
Взаимодействие
Усиливает эффект препаратов лития (в т.ч. токсичность), непрямых антикоагулянтов, пероральных гипогликемизирующих средств (производные сульфонилмочевины). Антациды снижают скорость всасывания. Одновременное применение др. НПВС увеличивает риск побочных явлений (особенно со стороны ЖКТ).
Меры предосторожности
С осторожностью назначают лицам пожилого возраста, на фоне диуретиков, нефротоксических препаратов, непосредственно после хирургических вмешательств. За несколько дней до хирургического вмешательства препарат следует отменить. В процессе длительного лечения необходим контроль функции печени и почек, протромбинового индекса (на фоне непрямых антикоагулянтов), глюкозы в крови (если пациент получает пероральные гипогликемизирующие средства).
Условия хранения
При температуре 15–25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Крылов Юрий Федорович
(фармаколог, доктор медицинских наук, профессор, академик Международной академии информатизации)
Опыт работы: более 34 лет
Упаковка
Суппозитории ректальные
Фармакологическое действие
Оказывает мощное и длительное болеутоляющее (наступает через 30 мин) и противовоспалительное действие при менее выраженном жаропонижающем. При ревматических заболеваниях ослабляет боль в суставах в покое и при движении, уменьшает утреннюю скованность и припухлость, улучшает функции и увеличивает объем движений суставов.
Показания к применению
Воспалительно-дегенеративные заболевания опорно-двигательного аппарата, сопровождающиеся болевым синдромом: суставной синдром при подагре, ревматоидный артрит, остеоартроз, анкилозирующий спондилоартрит, остеохондроз, суставной ревматизм (тендиниты, бурситы, миозиты), боли в позвоночнике, невралгии, миалгии, травмы.
Форма выпуска
суппозитории для ректального применения 20 мг; блистер 5, коробка (коробочка) 2;
Состав
1 таблетка, покрытая оболочкой, содержит теноксикама 20 мг; в коробке 3 блистера по 10 шт.
1 ректальный суппозиторий — 20 мг; в блистере 5 шт., в коробке 2 блистера.
Фармакодинамика
Оказывает мощное и длительное болеутоляющее (наступает через 30 мин) и противовоспалительное действие при менее выраженном жаропонижающее. При ревматических заболеваниях ослабляет боль в суставах в покое и при движении, уменьшает утреннюю скованность и припухлость, улучшает функции и увеличивает объем движений суставов.
Фармакокинетика
Быстро и полно всасывается в ЖКТ. Биодоступность 100%. C Max достигается через 2 часа.
Связывается с белками плазмы на 99%. Объем распределения — 0,15 л / кг. T1 / 2 — 60-75 час. В печени гидроксилюванню. Легко проходит гистогематические барьеры. Основная часть выводится в виде неактивных метаболитов с мочой, остальное — с желчью.
Использование во время беременности
Протипоказано.
Противопоказания к применению
Гиперчувствительность, активная пептическая язва, выраженные нарушения функции печени в активной стадии, почечная недостаточность, сахарный диабет, артериальная гипертензия, сердечная недостаточность, детский возраст.
Побочные действия
Тошнота, изжога, боли в животе, диарея, метеоризм, стоматит, анорексия, эрозивно-язвенные поражения, кровотечения, головная боль, головокружение, бессонница, депрессия, повышенная возбудимость, отек в области глаз, раздражение глаз, нарушение зрения, периферические отеки, повышение концентрации в плазме креатинина, мочевины азота, билирубина и активности печеночных трансаминаз, аллергические реакции (крапивница, зуд); при применении суппозиториев возможно местное раздражение, болезненная дефекация.
Способ применения и дозировка
Всередину, ректально. По 1 табл. або 1 супп. 1 раз на день (бажано в один і той же час).
При гострих нападах подагри по 2 табл. або 2 суп. 1 раз на добу протягом перших двох днів, потім по 1 табл. або 1 суп. 1 раз на день протягом 5 днів.
Взаимодействие с другими препаратами
Усиливает эффект препаратов лития (в т.ч. токсичность), непрямых антикоагулянтов, пероральных гипогликемических средств (производных сульфонилмочевины). Антациды снижают скорость всасывания.
Одновременное применение других. НПВС увеличивает риск побочных явлений (особенно со стороны ЖКТ).
Меры предосторожности
С осторожностью назначают лицам пожилого возраста, на фоне диуретиков, нефротоксических препаратов, непосредственно после хирургических вмешательств. За несколько дней до хирургического вмешательства препарат следует отменить. В процессе длительного лечения необходим контроль функции печени и почек, протромбинового индекса (на фоне непрямых антикоагулянтов), глюкозы в крови (если пациент получает пероральные гипогликемические средства).
Особые указания при приеме
Во время лечения необходим контроль картины периферической крови и функционального состояния печени и почек, протромбинового индекса (на фоне непрямых антикоагулянтов), концентрации глюкозы в крови (на фоне пероральных гипогликемических ЛС).
При необходимости определения 17-кетостероидов препарат следует отменить за 48 часов до исследования.
За несколько дней до хирургического вмешательства отменяют препарат. Необходимо учитывать возможность задержки Na + и воды в организме при назначении с диуретиками больным с артериальной гипертензией и ХСН. В период лечения необходимо соблюдать осторожность при вождении автотранспорта и занятии др. потенциально опасными видами деятельности, требующими повышенной концентрации внимания и скорости психомоторных реакций.
Условия хранения
Список Б.: При температурі 15-25 ° C.
Срок годности
36 мес.
Теноксикам
Теноксикам – эффективный, надежный, проверенный временем представитель группы нестероидных противовоспалительных препаратов (НПВП), который активно используется в мировой медицинской практике уже более 35 лет. С момента своего появления на фармакологическом рынке теноксикам прошел жесткую проверку в многочисленных сравнительных клинических исследованиях, выполненных по всем требованиям медицины, основанной на доказательствах, а также оценку длительного применения в реальной клинической практике в ходе серии национальных наблюдательных исследований. Его лечебный потенциал доказан при широком спектре ревматических заболеваний – остеоартрите, ревматоидном артрите, анкилозирующем спондилите, подагре, неспецифической боли в спине. Он также с успехом используется в хирургической практике для контроля послеоперационной боли и как компонент мультимодальной периоперационной анальгезии. Удобство применения (один раз в день), наличие различных лекарственных форм и хорошая переносимость (по сравнению с другими традиционными НПВП) делают теноксикам удачным инструментом обезболивающей терапии в самых разных отраслях медицины.
Нестероидные противовоспалительные препараты (НПВП) были и остаются незаменимым инструментом анальгетической и противовоспалительной терапии, востребованным в самых разных областях медицины. Лечение заболеваний суставов и позвоночника, купирование головной боли напряжения и мигрени, острой висцеральной боли («колики»), контроль болевого синдрома после травм и оперативных вмешательств, комплексная симптоматическая терапия онкологических больных и многое другое – области успешного использования этого класса фармакологических средств [1,3]. Это одна из наиболее обширных фармакологических групп: сегодня спектр НПВП, доступных российскому врачу, насчитывает более 20 международных непатентованных наименований, а число коммерческих препаратов (за счет генериков) превышает две сотни.
Такое разнообразие ставит врача перед непростым выбором – какой препарат назначить конкретному пациенту в той или иной клинической ситуации?
Формально, все НПВП обладают сходным обезболивающим и противовоспалительным потенциалом, разумеется, при условии, что они используются в максимальных терапевтических дозах в течение достаточно длительного времени. Это положение подтверждается обширным опытом «правильно организованных» с точки зрения медицины, основанной на доказательствах, рандомизированных контролируемых исследований (РКИ) [1,2]. Однако в реальной клинической практике на результат применения лекарства влияет множество факторов, связанных с характером заболевания, индивидуальной чувствительностью пациента и наличием коморбидной патологии. И, конечно, огромное значение имеют фармакологические особенности препарата, определяющие его быстродействие, стойкость эффекта и риск развития нежелательных реакций (НР) [3].
Одним из наиболее интересных биохимических семейств НПВП являются оксикамы. Они представляют собой производные эноликовой кислоты, которые, в отличие от большинства других НПВП, не содержат в своей структуре карбоксильную группу [4].
Общеизвестно, что главной фармакологической мишенью всех НПВП, независимо от химической структуры, является индуцируемый (т.е. появляющийся под воздействием провоспалительных цитокинов) фермент циклооксигеназа (ЦОГ)-2. Подавление активности этого фермента блокирует синтез простагландина (ПГ) Н2, который представляет собой субстрат для образования ПГЕ2, одного из наиболее важных медиаторов боли и воспаления [5,6]. ЦОГ – это последовательный гомодимер, белковая структура, объединяющая две взаимосвязанные зеркальные субъединицы, образующие при соприкосновении тонкий извитой гидрофобный канал, по которому происходит перемещение субстрата (полиненасыщенных жирных кислот, ПЖК) и где проходит его биохимическая трансформация. Оба мономера ЦОГ содержат N-терминальную зону (фактор роста подобную зону) – четырехспиральный участок, связанный с клеточной мембраной, и энзимный участок. В данной области ЦОГ имеются два участка: циклооксигеназный, где осуществляется окисление ПЖК и «замыкание» типичного для простаноидов циклопентанового кольца, и область пероксидазы, которая катализирует присоединение дополнительной OH- группы. Действие всех НПВП – от аспирина до коксибов, заключается в связывании циклооксигеназной области активной зоны ЦОГ, что нарушает ее взаимодействие с субстратом. Но пероксидазная активность фермента при этом не меняется [6,7].
Хотя все НПВП имеют общий механизм действия, разная биохимическая структура этих препаратов определяет важные отличия в их взаимодействии с ЦОГ. От этого зависит длительность их фармакологического эффекта и селективность в отношении ЦОГ-1/ЦОГ-2. Последнее имеет принципиальное значение: ведь именно с подавлением активности ЦОГ-2 связано анальгетическое, противовоспалительное и жаропонижающее действие НПВП. А неизбирательная блокада биохимического «двойника» этого фермента – ЦОГ-1, который постоянно присутствует в тканях организма и отвечает за синтез цитопротективных ПГ, приводит к развитию многих НР, таких как повреждение слизистой желудочно-кишечного тракта (ЖКТ) [4].
В чем особенность действия оксикамов? Они связываются с активной зоной ферментативного канала ЦОГ, образуя множественные гидрофобные связи и единственную непосредственную водородную связь между 4-гидроксильной группой молекулы препарата и аминокислотой Ser-530 ЦОГ. Фиксация двух молекул Н2О в активной зоне фермента обеспечивает дополнительные полярные связи между действующим веществом и структурами ЦОГ в каталитической вершине и области сужения ферментативного канала. Связь боковой цепи оксикама с аминокислотой Leu-531 ЦОГ формирует особую пространственную конформацию комплекса и появление гидрофобного «кармана», представленного 8 аминокислотными остатками фермента: Met-113, Val116, Leu-117, Ile-345, Val-349, Leu-531, Leu-534 и Me535. Согласно компьютерной модели взаимодействия оксикамов и ЦОГ, именно образование данной структуры определяет большую селективность в отношении ЦОГ-2 и более длительный противовоспалительный эффект этих препаратов [4].
Ценным свойством оксикамов представляется их способность влиять не только на активность ЦОГ-2, но и на матриксную ПГЕ2-синтетазу – фермент, благодаря которому происходит конечный синтез основного медиатора воспаления – ПГЕ2. Матриксная ПГЕ2-синтетаза является очень перспективной «мишенью» для противовоспалительной терапии, однако разработать пригодный для клинического применения ингибитор этого фермента («супер-НПВП») пока не удалось. В то же время оксикамы обладают структурным сходством с бензотиопиран S-диоксидами, а эти соединения могут связывать матриксную ПГЕ2-синтетазу и стали основой для создания экспериментального препарата PF-9184, показавшего свойство селективного ингибитора фермента [4].
Теноксикам – это надежный, проверенный временем лекарственный препарат, который широко используется во многих странах мира [8]. Впервые на фармакологическом рынке он появился в 1982 г. во Франции под торговым наименованием Тилкотил. В настоящее время, по данным сайта www.drugs.com, на глобальном фармакологическом рынке, кроме оригинального препарата, представлены еще 83 генерика теноксикама [9]. На 2016 г. теноксикам зарегистрирован и используется в 14 странах Евросоюза, таких как Бельгия, Болгария, Великобритания, Греция, Дания, Исландия, Испания, Италия, Кипр, Люксембург, Португалия, Румыния, Франция и Швеция [10].
Теноксикам относится к «традиционным» НПВП – неселективным ингибиторам ЦОГ-2. Соотношение ингибирующих концентраций ЦОГ-2/ЦОГ-1 для него составляет 1,34 (для примера, для индометацина – более 10) [11]. Имеются данные, что теноксикам, помимо своего основного фармакологического действия (блокада ЦОГ-2), способен проявлять свойства антиоксиданта, подавляя образование реактивных форм кислорода, супероксид-анионов, а также снижать синтез окиси азота [12-14].
Теноксикам обладает устойчивой стабильной фармакодинамикой. Он практически полностью всасывается из ЖКТ (биодоступность составляет 99%) и обнаруживается в крови уже через 30 мин после перорального приема. Достаточно быстро – в среднем через 1,9 ч (1,0-5,0 ч) после приема 20 мг теноксикама достигается пиковая концентрация препарата в плазме – 2,7 мг/л (2,3-3,0 мг/л). Теноксикам практически полностью связывается белками плазмы (на 99%), при этом, за счет низкой липофильности и высокой ионизации, его проникновение в ткани происходит плавно и постепенно: пиковая концентрация в синовиальной жидкости составляет 1/3 от содержания в плазме и достигается примерно через 20 ч. Препарат метаболизируется в печени с образованием 5′-гидрокси- и 6-O-глюкуронированной формы, которые выводятся с мочой и желчью. Особенностью теноксикама является линейная фармакодинамика (которая отмечается при использовании в дозах от 10 до 100 мг) и весьма медленная элиминация. Период полувыведения этого лекарства составляет 67 ч (49-81 ч) [8].
Теноксикам при хронических заболеваниях суставов и позвоночника
С момента появления на фармакологическом рынке теноксикам проходил жесткую проверку, прежде всего, как препарат, предназначенный для длительного использования у больных с хроническими ревматическими заболеваниями, такими как остеоартрит (ОА), ревматоидный
артрит (РА) и анкилозирующий спондилит.
С целью изучения эффективности и безопасности теноксикама была проведена серия масштабных и хорошо организованных РКИ. Так, в 12-недельной работе британских ученых теноксикам 20 мг/сут сравнивали с пироксикамом 20 мг/сут у 1328 больных ОА и РА [15]. Параллельно в Швейцарии было проведено РКИ, в котором оценивали действие теноксикама 20 мг/сут, пироксикама 20 мг/сут и диклофенака 100 мг/сут у пациентов с ОА и ревматической патологией околосуставных мягких тканей [16]. Третьей работой со сходным планом было 12-недельное РКИ датских исследователей, которые сопоставляли эффект теноксикама 20 мг/сут и кетопрофена 200 мг/сут у 307 больных ОА [17]. Во всех трех исследованиях был получен сходный результат: анальгетическое и противовоспалительное действие теноксикама не уступало препаратам контроля, но при этом суммарная частота НР, особенно со стороны ЖКТ, была ниже. Например, при сравнении теноксикама с кетопрофеном суммарная частота НР составила 29,0% и 47,3%, соответственно (p<0,05). Показательны данные N. Bellamy и соавт., которые сравнили результаты использования теноксикама 20 мг/сут и диклофенака 150 мг/сут у 98 больных ОА. Через 12 недель терапии не было отмечено существенного различия в динамике индекса WOMAC. Однако переносимость теноксикама была достоверно лучше таковой диклофенака: суммарная частота НР составила 43,8% и 66,0%, соответственно (p<0,05) [18].
Р. Riedemann и соавт. провели мета-анализ 18 РКИ, в 12 из которых теноксикам сравнивали с его ближайшим «родственником» пироксикамом, в 3 – с диклофенаком и в 2 – с индометацином. Согласно полученным данным, теноксикам был более эффективен и лучше переносился, чем пироксикам; он не уступал индометацину по эффективности и вызывал меньше НР; не отличался по лечебному потенциалу от диклофенака, но реже вызывал НР [19].
Для оценки клинических достоинств теноксикама, помимо РКИ, была проведена серия национальных наблюдательных исследований, в которых этот препарат изучали в реальной клинической практике. Например, в работе британских исследователей теноксикам применяли в течение 12 недель у 2963 больных ОА и РА. Препарат позволил успешно контролировать основные симптомы артрита (рис. 1). При этом около 60% пациентов продолжили использовать теноксикам более 3 мес, а 31% продлили его прием до 1 года [20].
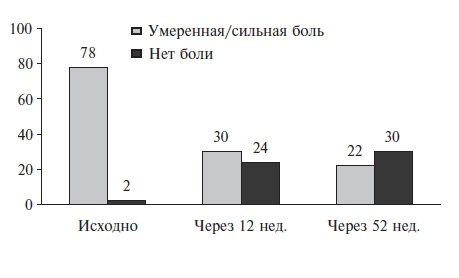
Рис. 1. Динамика боли (% пациентов) в суставах на фоне применения теноксикама 20 мг/сутки у 2963 больных ОА и РА (наблюдение 12 мес).
Адаптировано из [20]
Канадские ученые G. Kraag и соавт. провели масштабное наблюдательное исследование, в котором оценивали результаты использования теноксикама у 1809 амбулаторных больных с заболеваниями суставов и позвоночника, из которых большинство (84,3%) страдали ОА.
Средний курс терапии составил 4 недели. Теноксикам оказался эффективным и относительно безопасным лекарством. Так, 81,1% пациентов сообщили о существенном улучшении состояния после курса терапии, при этом лишь у 12,6% были отмечены те или иные
НР [21].
Итальянские ученые R. Marcolongo и A. Fioravanti оценили результаты применения теноксикама 20 мг/сут, диклофенака 100 мг/сут и пироксикама 20 мг/сут у 625 больных с ОА и ревматической патологией околосуставных мягких тканей. Теноксикам не уступал препаратам
контроля по эффективности, но превосходил по переносимости – частота НР при его применении оказалось самой низкой (7,4%) [22].
K. Ibrahima и соавт. изучали эффективность теноксикама 20 мг/сут (от 15 до 30 дней) у 736 африканских пациентов с ревматическими заболеваниями. Пода вляющее большинство больных (более 90%) оценили результат лечения как хороший или отличный [23].
Эффективность, хорошая переносимость и удобство применения сделали теноксикам удачным средством для длительного лечения больных с ревматическими заболеваниями. Это подтверждает опыт нескольких исследований, в которых лечебное действие теноксикама оценивали
в течение продолжительного периода времени. В частности, О. Nived и соавт. сравнивали теноксикам с напроксеном в течение 6 месяцев [24], а В. Lund и соавт. применяли теноксикам и пироксикам у больных ОА в течение 12 месяцев [25]. А в небольшом
исследовании J. Lalos и соавт. успешно использовали теноксикам в течение 4 лет (!) у 20 больных РА. При этом переносимость препарата была оценена как хорошая или отличная [26].
В плане оценки безопасности теноксикама очень важны результаты его сравнения с ацеклофенаком, который характеризуется хорошей переносимостью и низким риском серьезных НР. Испанские ученые провели два таких исследования. В работе F. Perez-Ruiz и соавт.
292 больных РА получали теноксикам 20 мг/сут или ацеклофенак 200 мг/сут в течение 3 мес. Эффективность препаратов через 2 недели и в конце исследования не различалась. Частота НР также была практически равной: 4,1% – в группе ацеклофенака и 6,2%
– в группе теноксикама. Число осложнений со стороны ЖКТ также достоверно не отличалось [27]. L. Villa Alcаzar и соавт. оценивали эффективность этих препаратов в аналогичных дозах при анкилозирующем спондилите (n=273). Через 3 мес лечения эффект
препаратов не отличался ни в отношении боли, ни в отношении улучшения функции позвоночника. При этом частота НР при лечении ацеклофенаком была несколько выше, чем при приеме теноксикама: они развились у 42 и 37 больных, соответственно. Частота
отмены двух препаратов из-за НР составила 2,2% и 1,4%, соответственно. Таким образом, в обоих исследованиях теноксикам не уступал по переносимости ацеклофенаку [28].
Эффективность теноксикама для купирования острой боли
Теноксикам представляет собой эффективное и удобное средство для длительного контроля основных симптомов при наиболее распространенных хронических заболеваниях суставов и позвоночника. Однако он может использоваться не только в этой ситуации. Теноксикам
оказался весьма удачным препаратом и для купирования острой боли при самой различной ургентной патологии.
Так, имеется успешный опыт применения теноксикама для лечения острого подагрического артрита [29,30]. Любопытно отметить, что теноксикам, согласно анализу Cochrane Collaboration, стал единственным НПВП, который сравнивали с плацебо для купирования острого
приступа подагры (de la Torre G., 1987). В этом РКИ 30 больных (по 15 в каждой группе) получали теноксикам 40 мг/сут или плацебо. По эффективности теноксикам значительно превосходил плацебо (рис.2). Очень важно, что в группе теноксикама не было
зафиксировано ни одной НР, в то время как в группе плацебо было 2 осложнения [31].
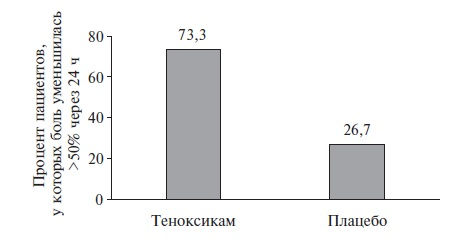
Рис. 2. Сравнение эффективности теноксикама и плацебо для купирования острого подагрического артрита.
Адаптировано из [31]
Теноксикам показал себя действенным средством для лечения острой неспецифической боли в спине. В работе бельгийских ученых М. Szpalski и J. Hayez 2-недельный курс лечения теноксикамом в дозе 20 мг у 78 пациентов с этой патологией привел к существенному
уменьшению боли и улучшению функции позвоночника [32].
Классической моделью для проверки терапевтического потенциала анальгетиков в ургентных ситуациях служит купирование острой боли после удаления зуба. Такую проверку прошел и теноксикам, причем очень успешно. Была проведена серия исследований, показавших
его эффективность в данной клинической ситуации [33-35]. При этом по уровню обезболивающего действия он не уступал большим дозам глюкокортикоидов [36] и превосходил мягкие опиоидные препараты (в частности, комбинацию парацетамола 500 мг и кодеина
8 мг) [37].
В качестве примера удачного использования теноксикама в стоматологической практике можно привести РКИ J. Roelofse и соавт., в которое были включены 35 пациентов, перенесших удаление 3-го моляра. Теноксикам сравнивали с диклофенаком: оба препарата вводили
непосредственно перед операцией (теноксикам 40 мг внутривенно, диклофенак 75 мг внутримышечно), а затем назначали внутрь (теноксикам 20 мг один раз в день, диклофенак 50 мг три раза в день) на 7 дней. Эффективность теноксикама оказалась достоверно
выше как в первые послеоперационные часы, так и через 3 дня (рис. 3) [38].
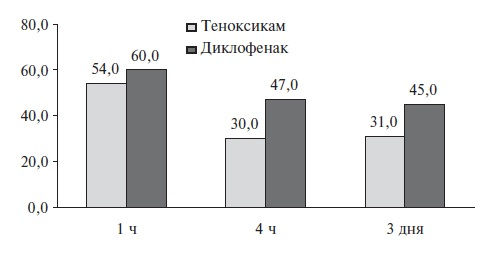
Рис. 3. Сравнение эффективности тенкосикама и диклофенака при купировани боли после экстракции зуба (выраженность боли в мм ВАШ).
Адаптировано из [38]
Эффективность теноксикама для купирования боли после экстракции зуба подтверждает также недавнее исследование V. Kaplan и соавт. у 90 больных, перенесших удаление зуба мудрости. В качестве анальгетика они в течение 7 дней получали теноксикам 20 мг, флурбипрофен
200 мг или диклофенак 100 мг, причем первую доза каждого препарата назначали за 2 ч до операции. Теноксикам оказывал более выраженное обезболивающее действие по сравнению с препаратами сравнения как в первые послеоперационные часы, так и последующие
дни наблюдения [39].
Важнейшая область ургентного применения НПВП – купирование острой почечной и билиарной колики. Здесь теноксикам также показал себя эффективным препаратом: внутривенное или внутримышечное введение препарата быстро и существенно снижало выраженность болевых
ощущений и частоту осложнений, связанных с этой патологией [40-44].
Теноксикам применяется в анестезиологической практике как элемент мультимодального обезболивания при «больших» хирургических операциях. Его эффективность была подтверждена результатами серии РКИ. Так, в работе W. Chang и соавт. предоперационное введение
этого препарата обеспечивало снижение потребности в применении опиоидов в послеоперационном периоде у больных, перенесших хирургическое вмешательство на позвоночнике [45]. Очень важные данные были получены I. Gunusen и соавт., которые сравнили
выраженность боли и потребность в морфине у 120 больных, которые после абдоминальной гистерэктомии получали внутривенно теноксикам 20 мг, парацетамол 1 г или плацебо. В группе теноксикама послеоперационная боль была достоверно менее выражена,
а суммарная потребность в морфине в трех группах составила 44,8±17,4 мг, 64,6±19,6 мг и 69,2±22,1 мг, соответственно (p<0,05) [46]. Снижение потребности в морфине при использовании теноксикама после холецистэктомии было также показано в исследовании
F. Munro и соавт [47].
T. Akca и соавт. сравнили эффекты предоперационного введения 20 мг теноксикама или физиологического раствора у 80 больных, которым была проведена лапароскопическая холецистэктомия или пластика паховой грыжи. В группе теноксикама выраженность боли через
4 и 8 ч после операции, а также потребность в дополнительных анальгетиках оказалась достоверно ниже, чем в контрольной группе [48].
А. Merry и соавт. оценивали влияние интраоперационного внутривенного введения теноксикама 20 и 40 мг или плацебо на выраженность послеоперационной боли у 45 больных, перенесших торакотомию. Выраженность боли оказалась достоверно меньше при использовании
обеих доз теноксикама: 17,4±14,8, 16,5±13,3 и 25,8±12,5 мм по визуальной аналоговой шкале, соответственно (p<0,05) [49].
Нельзя обойти вниманием еще одну область клинического применения теноксикама – его локальное внутри- и околосуставное введение при патологии суставов или околосуставных мягких тканей. Хотя такое применение теноксикама не зарегистрировано, тем не менее,
оно активно практикуется в ряде стран мира [50]. Так, Z. Unlu и соавт. сравнили эффект внутрисуставного введения теноксикама 20 мг (три еженедельные инъекции) и постоянного перорального приеме этого препарата в течение 3 недель у 69 больных ОА
коленного сустава. Оба метода применения позволили добиться существенного улучшения состояния больных, причем выраженность боли в обеих группах достоверно не различалась через 1, 3 и 6 мес [51]. Недавно были представлены данные аналогичного по
плану исследования, выполненного М. Erbas и соавт. В нем также сравнивали результаты 3-недельного внутрисуставного и перорального применения теноксикама у 60 больных ОА. Как и в предыдущем исследовании, эффективность лечения не отличалась [52].
В исследовании Н. Çift и соавт. 40 больных с тендинитом ротаторов плеча и/или субакромиальным бурситом получали внутрисуставные инъекции метилпреднизолона 40 мг (однократно) или теноксикама 20 мг (3 инъекции еженедельно). Эффект двух препаратов был сходным:
через 6 недель в группе метилпреднизолона интенсивность боли снизилась с 6,2 до 3,6 см (по визуальной аналоговой шкале длиной 10 см), в группе теноксикама – с 7,8 до 2,6 см [53].
S. Guner и соавт. сравнили результаты локального введения теноксикама 20 мг и метилпреднизолона 40 мг (оба препарата в комбинации с 2% лидокаином) у 61 пациента с плантарным фасциитом. Оба препарата были эффективными и вызывали сопоставимое уменьшение
боли через 6 и 12 ч после инъекции [54]. С другой стороны, в работе S. Karthikeyan и соавт. было показано преимущество однократной субакромиальной инъекции метилпреднизолона перед однократным субакромиальным введением теноксикама 20 мг при синдроме
столкновения ротаторов плеча [55].
Некоторые хирурги-ортопеды активно практикуют внутрисуставное введение теноксикама с опиоидами и локальными анестетиками после артроскопических вмешательств на суставах (например, после менискэктомии). Имеются четкие данные, что использование теноксикама
в этой ситуации позволяет существенно уменьшить послеоперационную боль [56-58]. Напри мер, R. Jawish и соавт. выявлили значительное уменьшение воспалительного отека и боли у 134 больных, которым в конце артроскопии коленного сустава внутрисуставно
вводили теноксикам 20 мг [59].
Очень интересные данные были получены S. Sanel и соавт. в ходе двойного слепого РКИ, в котором были сопоставлены эффекты теноксикама 20 мг и морфина (оба препарата применяли в комбинации с 0,5% бупивокаином) у 240 больных, перенесших артроскопическое
вмешательство на коленном суставе. Применение теноксикама позволило добиться меньшего уровня послеоперационной боли и снижения потребности в дополнительных анальгетиках по сравнению с применением опиоида [60].
Безопасность
Как было отмечено выше, теноксикам относится к «традиционным» НПВП, т.е. неселективным ингибиторам ЦОГ-2, поэтому на фоне приема этого препарата могут отмечаться НР, свойственные всем другим представителям этой лекарственной группы. Прежде всего, речь
идет о возможности развития осложнений со стороны ЖКТ [61]. Тем не менее, согласно данным многочисленных РКИ и наблюдательных исследований, приведенных выше, по переносимости он в целом превосходит многие другие популярные НПВП [19].
Было проведено несколько исследований, в которых изучалось действие теноксикама на слизистую оболочку верхних отделов ЖКТ. Так, Р. Müller и соавт. сравнили частоту эндоскопических изменений после 14-дневного приема теноксикама 20 мг/сут и диклофенака
100 мг/сут у 36 здоровых добровольцев. Теноксикам достоверно реже вызывал повреждения слизистой оболочки. Так, счет Lanza, отражающий выраженность изменений, составил 1,3±0,7 и 2,2±1,1 в двух группах, соответственно (р=0,014) [62]. А. al-Quorain
и соавт. сравнивали частоту изменений слизистой оболочки желудка у 36 больных, получавших теноксикам 20 мг и диклофенак 100 мг в течение 4 недель. Повреждение слизистой оболочки было отмечено у 21% и 41% больных, соответственно. При этом множественные
геморрагии и эрозии (>10) были выявлены лишь у 5% больных, получавших теноксикам, и 18% пациентов группы диклофенака [63].
G. Perpignano и соавт. оценили частоту и характер эндоскопических изменений ЖКТ у 60 больных ОА, которые в течение 8 недель получали теноксикам 20 мг/сут или умеренно селективный НПВП с хорошей переносимостью этодолак 600 мг/сут. Частота минимальных изменений
слизистой желудка оказалась выше в группе теноксикама, однако язвы желудка встречались с одинаковой частотой (по 2 в каждой группе) [64].
Важные данные о сравнительной частоте НР при использовании теноксикама в реальной клинической практике были получены специалистами французской системы фармаконадзора, которые оценили 42389 спонтанных сообщений о серьезных НР, зарегистрированных за период
с 2002 по 2006, и построили «рейтинг» для наиболее популярных НПВП в зависимости от частоты лекарственных осложнений. При лечении теноксимамом частота НР была низкой (0,42 случая на 1 млн принятых доз), сопоставимой с таковой при применении мелоксикама
(0,41) и существенно ниже, чем при лечении диклофенаком (0,58) и особенно кетопрофеном (0,78) [65].
Данные по осложнениям со стороны сердечнососудистой системы при применении теноксикама ограничены, однако другие представители семейства оксикамов (мелоксикам и пироксикам) характеризуются средним риском их развития [66,67]. Недавно А. Arfе и соавт. провели
анализ взаимосвязи между приемом НПВП и развитием сердечной недостаточности у 92163 больных, госпитализированных в связи с этой патологией в Нидерландах, Германии, Велико британии и Италии за период с 2000 по 2010 гг. Соответствующую по полу и
возрасту контрольную группу составили 8 246 403 пациента без сердечной недостаточности. В среднем, прием НПВП ассоциировался с умеренным нарастанием риска сердечной недостаточности: показатель относительного риска (ОР) составил 1,19 (95% доверительный
интервал [ДИ] 1,17-1,22). Теноксикам практически не повышал риск развития сердечной недостаточности (ОР 1,06; 95% ДИ 0,80-1,41). Для диклофенака этот показатель составил 1,19 (95% ДИ 1,151,24) [67].
Разумеется, при использовании теноксикама следует учитывать все противопоказания и тщательно оценивать наличие факторов риска класс-специфических осложнений, свойственных НПВП.
Заключение
Теноксикам – универсальный НПВП, который может использоваться как для купирования острой боли (в том числе в хирургической практике), так и и для длительного контроля болевых ощущений при хронических заболеваниях суставов и позвоночника. Имеется обширная
доказательная база, основанная на данных хорошо организованных клинических испытаний и многолетнем опыте реальной практической работы, подтверждающая эффективность и хорошую переносимость этого препарата. Он удобен в применении (назначают один
раз в день) и имеет различные лекарственные формы, в том числе для парентерального введения. Эти достоинства определяют целесообразность активного использования теноксикама в российской медицинской практике.
Используемые источники
- Brune K, Patrignani P. New insights into the use of currently available nonsteroidal anti-inflammatory drugs. J Pain Res 2015;8:105-18.
- Conaghan PG. A turbulent decade for NSAIDs: update on current concepts of classification, epidemiology, comparative efficacy, and toxicity. Rheumatol Int 2012;32(6):1491-502.
- Hunter TS, Robison C, Gerbino PP. Emerging evidence in NSAID pharmacology: important considerations for product selection. Am J Manag Care 2015;21(7 Suppl):S139-47.
- Xu S, Rouzer CA, Marnett LJ. Oxicams, a class of nonsteroidal anti-inflammatory drugs and beyond. IUBMB Life 2014;66(12):803-11.
- Díaz-González F, Sаnchez-Madrid F. NSAIDs: learning new tricks from old drugs. Eur J Immunol 2015;45(3):679-86.
- Vecchio AJ, Malkowski MG. The structural basis of endocannabinoid oxygenation by cyclooxygenase-2. J Biol Chem 2011;286(23):20736-45.
- Vecchio AJ, Simmons DM, Malkowski MG. Structural basis of fatty acid substrate binding to cyclooxygenase-2. J Biol Chem 2010;285(29):22152-63.
- Nilsen OG. Clinical pharmacokinetics of tenoxicam. Clin Pharmacokinet 1994;26(1):16-43.
- https://www.drugs.com/international/tenoxicam.html.
- http://www.ema.europa.eu/docs/en_GB/document_library/Periodic_safety_update_single_assessment/2016/10/WC500214741.pdf.
- Lora M, Morisset S, Mеnard HA, et al. Expression of recombinant human cyclooxygenase isoenzymes in transfected COS-7 cells in vitro and inhibition by tenoxicam, indomethacin and aspirin. Prostaglandins Leukot Essent Fatty Acids 199;56(5):361-7.
- Van Antwerpen P, N ève J. In vitro comparative assessment of the scavenging activity against three reactive oxygen species of non-steroidal anti-inflammatory drugs from the oxicam and sulfoanilide families. Eur J Pharmacol 2004;496(13):55-61.
- Ferrari GV, Natera J, Paulina Monta ña M Scavenging of photogenerated ROS by Oxicams. Possible biological and environmental implications. J Photochem Photobiol B 2015;153:233-9.
- Ozgocmen S, Ardicoglu O, Erdogan H, et al. In vivo effect of celecoxib and tenoxicam on oxidant/ anti-oxidant status of patients with knee osteoarthritis. Ann Clin Lab Sci 2005;35(2):137-43.
- Simpson J, Golding DN, Freeman AM, et al. A large multicentre, parallel group, double-blind study comparing tenoxicam and piroxicam in the treatment of osteoarthritis and rheumatoid arthritis. Br J Clin Pract 1989;43(9):328-33.
- Moser U, Waldburger H, Schwarz HA, Gobelet CA. A double-blind randomised multicentre study with tenoxicam, piroxicam and diclofenac sodium retard in the treatment of ambulant patients with osteoarthritis and extra-articular rheumatism. Scand J Rheumatol Suppl 1989;80:71-80.
- Ejstrup L, Knudsen JV, Petersen L. A randomised double-blind multicentre trial comparing tenoxicam and ketoprofen in osteoarthritis. Scand J Rheumatol Suppl 1989;80:48-53.
- Bellamy N, Buchanan WW, Chalmers A, et al. A multicenter study of tenoxicam and diclofenac in patients with osteoarthritis of the knee. J Rheumatol 1993;20(6):999-1004.
- Riedemann PJ, Bersinic S, Cuddy LJ, et al. A study to determine the efficacy and safety of tenoxicam versus piroxicam, diclofenac and indomethacin in patients with osteoarthritis: a meta-analysis. J Rheumatol 1993;20(12):2095-103.
- Langdon CG, Moran DG, Jamieson V, et al. A multicentre study of tenoxicam review5_Layout 1 18.11.17 19:47 Page 49
- Kraag GR, Gordon DA, M énard HA, et al. Patient compliance with tenoxicam in family practice. Clin Ther 1994;16(3):581-93.
- Marcolongo R, Fioravanti A. Clinical experiences with tenoxicam. Preliminary results of a multicenter study. Recenti Prog Med 1991;82(4):242-9.
- Ibrahima K, Kodjo G, Issa S, et al. Clinical efficacy and tolerability of tenoxicam in African patients with osteoarthritis, rheumatoid arthritis, tendinitis and/or bursitis: an open study. Curr Med Res Opin 1991;12(7):471-8.
- Nived O, Sturfelt G, Eckern äs SA, Singer P. A comparison of 6 months’ compliance of patients with rheumatoid arthritis treated with tenoxicam and naproxen. Use of patient computer data to assess response to treatment. J Rheumatol 1994;21(8):1537-41.
- Lund B, Andersen RB, Fossgreen J, et al. A long-term randomised trial on tenoxicam and piroxicam in osteoarthritis of the hip or knee: a 24-month interim report focusing on the 12-24 month interval. Eur J Rheumatol Inflamm 1987;9(2):58-67.
- Lalos J, Tsachalos P, Gallis L. Long-term (four year) clinical trial with tenoxicam and basis therapy in patients suffering from rheumatoid arthritis. Scand J Rheumatol Suppl 1989;80:67-70.
- Perez-Ruiz F, Alonso-Ruiz A, Ansoleaga JJ. Comparative study of the efficacy and safety of aceclofenac and tenoxicam in rheumatoid arthritis. Clin Rheumatol 1996;15(5):473-7.
- Villa Alc ázar LF, de Buergo M, Rico Lenza H, Montull Fruit ós E. Aceclofenac is as safe and effective as tenoxicam in the treatment of ankylosing spondylitis: a 3 month multicenter comparative trial. Spanish Study Group on Aceclofenac in Ankylosing Spondylitis. J Rheumatol 1996;23(7):1194-9.
- Vald és EF. Use of tenoxicam in patients with acute gouty arthritis. Eur J Rheumatol Inflamm 1987;9(2):133-6.
- Waterworth RF, Waterworth SM. An open assessment of tenoxicam (Tilcotil) in the treatment of acute gout in general practice. N Z Med J 1987;100(837):744-5.
- van Durme CM, Wechalekar MD, Buchbinder R, et al. Non-steroidal antiinflammatory drugs for acute gout. Cochrane Database Syst Rev 2014;(9):CD010120.
- Szpalski M, Hayez JP. Objective functional assessment of the efficacy of tenoxicam in the treatment of acute low back pain. A double-blind placebo-controlled study. Br J Rheumatol 1994;33(1):74-8.
- Cheung LK, Rodrigo C. Tenoxicam for pain relief following third molar surgery. Anesth Pain Control Dent 1992;1(4):229-33.
- Zacharias M, De Silva RK, Herbison P, Templer P. A randomized crossover trial of tenoxicam compared with rofecoxib for postoperative dental pain control. Anaesth Intensive Care 2004;32(6):770-4.
- Arslan H, Topcuoglu HS, Aladag H. Effectiveness of tenoxicam and ibuprofen for pain prevention following endodontic therapy in comparison to placebo: a randomized double-blind clinical trial. J Oral Sci 2011;53(2):157-61.
- Ilhan O, Agacayak KS, Gulsun B, et al. A comparison of the effects of methylprednisolone and tenoxicam on pain, edema, and trismus after impacted lower third molar extraction. Med Sci Monit 2014;20:147-52.
- Merry AF, Swinburn PF, Middleton NG, et al. Tenoxicam and paracetamolcodeine combination after oral surgery: a prospective, randomized, double-blind, placebo-controlled study. Br J Anaesth 1998;81(6):875-80.
- Roelofse JA, Van der Bijl P, Joubert JJ. Analgesic and anti-inflammatory efficacy of tenoxicam and diclofenac sodium after third molar surgery. Anesth Prog 1996;43(4):103-7.
- Kaplan V, Ero ğlu CN. Comparison of the effects of daily single-dose use of flurbiprofen, diclofenac sodium, and tenoxicam on postoperative pain, swelling, and trismus: a randomized double-blind study. J Oral Maxillofac Surg 2016;74(10):1946.e1-6.
- Cevik E, Cinar O, Salman N, et al. Comparing the efficacy of intravenous tenoxicam, lornoxicam, and dexketoprofen trometamol for the treatment of renal colic. Am J Emerg Med 2012;30(8):1486-90.
- Keke çZ, Yilmaz U, S özüer E. The effectiveness of tenoxicam vs isosorbide dinitrate plus tenoxicam in the treatment of acute renal colic. BJU Int 2000;85(7):783-5.
- al-Waili NS, Saloom KY. Intravenous tenoxicam to treat acute renal colic: comparison with buscopan compositum. J Pak Med Assoc 1998;48(12):370-2.
- Al-Waili NS. Intramuscular tenoxicam to treat acute renal colic. Br J Urol 1996;77(1):15-6.
- Masudi T, Capitelli-McMahon H, Anwar S. Acute pain management in symptomatic cholelithiasis. World J Gastrointest Surg 2016;8(10):713-8.
- Chang WK, Wu HL, Yang CS, et al. Effect on pain relief and inflammatory response following addition of tenoxicam to intravenous patient-controlled morphine analgesia: a double-blind, randomized, controlled study in patients undergoing spine fusion surgery. Pain Med 2013;14(5):736-48.
- Gunusen I, Karaman S, Acar A, et al. The efficacy of paracetamol versus tenoxicam on postoperative pain and morphine consumption after abdominal hysterectomy: a placebo-controlled, randomized study. Clin Exp Obstet Gynecol 2012;39(1):49-52.
- Munro FJ, Young SJ, Broome IJ, et al. Intravenous tenoxicam for analgesia following laparoscopic cholecystectomy. Anaesth Intensive Care 1998;26(1):56-60.
- Akca T, Colak T, Kanik A, et al. The effect of preoperative intravenous use of tenoxicam: a prospective, double-blind, placebo-controlled study. J Invest Surg 2004;17(6):333-8.
- Merry AF, Sidebotham DA, Middleton NG, et al. Tenoxicam 20 mg or 40 mg after thoracotomy: a prospective, randomized, double-blind, placebo-controlled study. Anaesth Intensive Care 2002;30(2):160-6.
- Papathanassiou NP. Intra-articular use of tenoxicam in degenerative osteoarthritis of the knee joint. J Int Med Res 1994;22(6):332-7.
- Unlu Z, Ay K, Tuzun C. Comparison of intra-articular tenoxicam and oral tenoxicam for pain and physical functioning in osteoarthritis of the knee. Clin Rheumatol 2006;25(1):54-61.
- Erbas M, Simsek T, Kiraz HA et al. Comparison of the effectivity of oral and intra-articular administration of tenoxicam in patients with knee osteoarthritis. Braz J Anesthesiol 2015;65(5):333-7.
- Çift H, Özkan F Ü, Tolu S, et al. Comparison of subacromial tenoxicam and steroid injections in the treatment of impingement syndrome. Eklem Hastalik Cerrahisi 2015;26(1):16-20.
- Guner S, Onder H, Guner SI et al. Effectiveness of local tenoxicam versus corticosteroid injection for plantar fasciitis treatment. Orthopedics 2013;36:e1322-6.
- Karthikeyan S, Kwong HT, Upadhyay PK, et al. A double-blind randomised controlled study comparing subacromial injection of tenoxicam or methylprednisolone in patients with subacromial impingement. J Bone Joint Surg Br 2010;92(1):77-82.
- Cook TM, Tuckey JP, Nolan JP. Analgesia after day-case knee arthroscopy: double-blind study of intra-articular tenoxicam, intra-articular bupivacaine and placebo. Br J Anaesth 1997;78(2):163-8.
- Talu GK, Ozyal çin S, Koltka K, et al. Comparison of efficacy of intraarticular application of tenoxicam, bupivacaine and tenoxicam: bupivacaine combination in arthroscopic knee surgery. Knee Surg Sports Traumatol Arthrosc 2002;10:355-60.
- Oral EG, Hanci A, Ulufer Sivrikaya G et al. The analgesic effects of morphine and tramadol added to intra-articular levobupivacaine-tenoxicam combination for arthroscopic knee surgery on postoperative pain; a randomized clinical trial. Anesth Pain Med 2015;5(3):e24047.
- Jawish R, Najdi H, Abi Safi C, Chameseddine A. The effect of intra-articular Tenoxicam on knee effusion after arthroscopy. Int Orthop 2015;39(7):1423-6.
- Sanel S, Arpaz O, Unay K, et al. Comparison of intra-articular bupivacaine-morphine with bupivacaine-tenoxicam combinations on post-operative analgesia in patients with arthroscopic meniscectomy: a prospective, randomised study. Int Orthop 2016;40(3):601-5.
- Castellsague J, Riera-Guardia N, Calingaert B, et al. Individual NSAIDs and upper gastrointestinal complications: a systematic review and meta-analysis of observational studies (the SOS project). Drug Saf 2012;35(12):1127-46.
- Müller P, Dammann HG, Marinis E, Simon B. Gastroduodenal tolerance of tenoxicam versus diclofenac-Na: an endoscopy double-blind controlled study in healthy probands. Z Rheumatol 1989;48(5):243-5.
- al-Quorain AA1, Satti MB, Marwah S, et al. Non-steroidal anti-inflammatory drug-induced gastropathy: a comparative endoscopic and histopathological evaluation of the effects of tenoxicam and diclofenac. J Int Med Res 1993;21(2):89-97.
- Perpignano G, Bogliolo A, Puccetti L. Double-blind comparison of the efficacy and safety of etodolac SR 600 mg u.i.d. and of tenoxicam 20 mg u.i.d. in elderly patients with osteoarthritis of the hip and of the knee. Int J Clin Pharmacol Res 1994;14(5-6):203-16.
- Lapeyre-Mestre M, Grolleau S, Montastruc JL. Adverse drug reactions associated with the use of NSAIDs: a case/noncase analysis of spontaneous reports from the French pharmacovigilance database 2002-2006. Fundam Clin Pharmacol 2013; 27(2):223-30.
- McGettigan P, Henry D. Cardiovascular risk and inhibition of cyclooxygenase: a systematic review of the observational studies of selective and nonselective inhibitors of cyclooxygenase 2. JAMA 2006;296(13):1633-44.
- Varas-Lorenzo С, Riera-Guardia N, Calingaert B, et al. Myocardial infarction and individual nonsteroidal anti-inflammatory drugs meta-analysis of observational studies. Pharmacoepidemiol Drug Saf 2013;22:559–70.
- Arfe A, Scotti L, Varas-Lorenzo C, et al. Non-steroidal anti-inflammatory drugs and risk of heart failure in four European countries: nested case-control study. BMJ 2016;354:i4857
Версия на английском языке
МНН: Теноксикам
Производитель: «Уорлд Медицин Илач Сан. ве Тидж. А.Ш.»
Анатомо-терапевтическо-химическая классификация: Tenoxicam
Номер регистрации в РК:
РК-ЛС-5№023231
Информация о регистрации в РК:
09.09.2022 — 09.09.2032
- русский
- қазақша
- Скачать инструкцию медикамента
Торговое название
Артоксан
Международное непатентованное название
Теноксикам
Лекарственная форма
Таблетки,
покрытые пленочной оболочкой
Состав
Одна
таблетка содержит
Активное
вещество:
теноксикам 20 мг,
Вспомогательные
вещества: лактозы
моногидрат, крахмал кукурузный прежелатинизированный, тальк, магния
стеарат,
Состав
оболочки: опадри
желтый 02F22025 (гипромеллоза, титана диоксид (Е171), макрогол 6000,
железа оксид желтый (Е172), тальк.
Описание
Таблетки
круглой формы, покрытые пленочной оболочкой желтого цвета,
двояковыпуклые.
Фармакотерапевтическая группа
Препараты
для лечения заболеваний костно-мышечной системы.
противовоспалительные и противоревматические препараты. Нестероидные
противовоспалительные препараты. Оксикамы. Теноксикам.
Код АТС M01AC02
Фармакологические свойства
Фармакокинетика
Теноксикам
быстро и полностью всасывается из желудочно-кишечного тракта (ЖКТ),
прием пищи и антацидов замедляет скорость абсорбции, не влияя на
общую степень всасывания. Максимальная концентрация в плазме крови
достигается через 2 часа. Биодоступность 100%. Препарат на 99%
связывается с белками плазмы. Отличительной особенностью теноксикама
является большая продолжительность действия и длительный период
полувыведения — 72 часа. Теноксикам хорошо проникает в синовиальную
жидкость. Легко проникает через гистогематические барьеры.
Подвергается трансформации в печени с образованием неактивных
метаболитов. Средний период полувыведения составляет 60-75 часов.
Экскреция реализуется преимущественно с мочой и частично с желчью.
Фармакодинамика
Артоксан
— эффективный нестероидный противовоспалительный препарат (НПВП) с
мощным противовоспалительным, анальгезирующим и умеренным
жаропонижающим действием. Свойства препарата обусловлены
ингибированием обеих изоформ фермента циклооксигеназы, что приводит к
нарушению метаболизма арахидоновой кислоты и блокаде синтеза
простагландинов.
Противовоспалительный
эффект обусловлен уменьшением проницаемости капилляров (ограничивает
экссудацию), стабилизацией лизосомальных мембран (препятствует выходу
ферментов лизосом, вызывающих повреждение тканей), угнетением синтеза
или инактивацией медиаторов воспаления (простагландинов, гистамина,
брадикинина, лимфокинов, факторов комплемента). Уменьшает количество
свободных радикалов в очаге воспаления, угнетает хемотаксис и
фагоцитоз. Тормозит пролиферативную фазу воспаления, уменьшает
поствоспалительное склерозирование тканей. Оказывает
хондропротекторное действие.
Препарат
купирует или снижает интенсивность болевого синдрома любой этиологии,
уменьшает утреннюю скованность, увеличивает подвижность пораженных
суставов. При продолжительном применении оказывает
десенсибилизирующее действие.
Особенностью
теноксикама является продолжительное действие.
Показания к применению
—
облегчение боли и воспаления при остеоартрите и ревматоидном артрите;
—
краткосрочное лечение острых заболеваний опорно-двигательного
аппарата, включая растяжения, вывихи и другие повреждения мягких
тканей.
Способ применения и дозы
Артоксан
принимают внутрь.
Предпочтительно
принимать во время или после приема пищи.
Препарат
назначают в дозе 20 мг 1 раз в сутки в одно и то же время.
Следует
избегать назначения более высоких доз, поскольку достижения
клинически значимого эффекта не наблюдается, вместе с тем повышается
риск развития побочных реакций.
Обычно
препарат принимается не более 7 дней, но в тяжелых случаях возможно
применение максимум до 14 дней.
Побочные действия
Наблюдавшиеся
нежелательные эффекты обычно являлись слабыми и преходящими. У
небольшого количества пациентов требовалось прекращение лечения по
причине нежелательных эффектов.
Внутри
классов согласно классификации поражений систем и органов
неблагоприятные реакции перечислены согласно частоте (количеству
пациентов, у которых ожидается возникновение данной реакции) с
применением следующих обозначений:
Очень
часто (≥1/10)
Часто
(от ≥1/100 до <1/10)
Нечасто
(от ≥1/1000 до <1/100)
Редко
(от ≥1/10000 до <1/1000)
Очень
редко (<1/10000)
Частота
неизвестна (оценка на основании имеющихся данных невозможна).
Нарушения
со стороны крови и лимфатической системы
Частота
неизвестна: агранулоцитоз, анемия, апластическая анемия,
гемолитическая анемия, лейкопения, тромбоцитопения,
нетромбоцитопеническая пурпура, эозинофилия.
Нарушения
со стороны иммунной системы
Частота
неизвестна: реакции гиперчувствительности, такие как астма,
анафилактические реакции, ангионевротический отек.
Нарушения
метаболизма и питания
Часто:
анорексия.
Редко:
нарушения метаболизма (например: гипергликемия, увеличение/снижение
массы тела).
Нарушения
психики
Редко:
нарушения сна (например, бессонница), депрессия, нервозность,
аномальные сны.
Частота
неизвестна: спутанность сознания, галлюцинации.
Нарушения
со стороны нервной системы
Часто:
головокружение, головная боль.
Частота
неизвестна: сонливость, парестезии.
Нарушения
со стороны органа зрения
Частота
неизвестна: нарушения зрения (такие как снижение остроты зрения и
помутнение зрения), опухание глаз, раздражение глаз.
Нарушения
со стороны органа слуха и равновесия
Редко:
вертиго.
Частота
неизвестна: шум в ушах.
Нарушения
со стороны сердца
Редко:
учащенное сердцебиение.
Частота
неизвестна: сердечная недостаточность
Необходимо
учитывать вероятность провоцирования застойной сердечной
недостаточности у пожилых пациентов и пациентов с нарушением функции
сердца.
Нарушения
со стороны сосудов
Редко:
тромботические явления (например, инфаркт миокарда или инсульт).
Частота
неизвестна: васкулит, гипертензия.
Результаты
клинических и эпидемиологических исследований показывают, что
применение селективных ингибиторов циклооксигеназы-2 (ингибиторов
ЦОГ-2) и некоторых НПВС (в особенности при высоких дозах и в течение
длительного времени) может приводить к небольшому повышению риска
возникновения артериальных тромботических явлений (например, инфаркта
миокарда или инсульта). Несмотря на то, что теноксикам не увеличивал
частоту возникновения тромботических явлений, таких как инфаркт
миокарда, имеющиеся данные являются недостаточными для исключения
подобного риска для теноксикама.
Нарушения
со стороны органов дыхания, грудной клетки и средостения
Редко:
бронхоспазм, осложненная астма, одышка.
Частота
неизвестна: носовое кровотечение.
Бронхоспазм
и осложненная астма наблюдались при лечении НПВС.
Нарушения
со стороны желудочно-кишечного тракта
Очень
часто: боль и дискомфорт в желудке, эпигастральной области и брюшной
полости, диспепсия, тошнота, рвота, метеоризм, запор, несварение,
эпигастральный дискомфорт, стоматит.
Часто:
желудочно-кишечное кровотечение, перфорация желудочно-кишечного
тракта, язва желудочно-кишечного тракта, пептическая язва, иногда с
летальным исходом, в особенности у пожилых пациентов, кровавая рвота,
стул с кровью, запор, изъязвление полости рта, гастрит, сухость во
рту, обострение колита и болезни Крона (см. раздел 4.4 «Особые
предупреждения и меры предосторожности при использовании»).
Очень
редко: панкреатит.
Нарушения
со стороны печени и желчевыводящих путей
Нечасто:
повышение уровней печеночных ферментов.
Частота
неизвестна: гепатит, желтуха.
Нарушения
со стороны кожи и подкожной ткани
Нечасто:
зуд, эритема, экзантема, сыпь, крапивница.
Редко:
везикуло-буллезные реакции.
Очень
редко: тяжелые неблагоприятные кожные реакции (ТНКР): синдром
Стивенса-Джонсона, токсический эпидермальный некролиз.
Частота
неизвестна: реакция фоточувствительности.
Сообщалось
о редких случаях возникновения нарушений со стороны ногтей и реакций
фоточувствительности после лечения НПВС.
Нарушения
со стороны почек и мочевыводящих путей
Нечасто:
повышение уровней мочевины или креатинина в крови.
Частота
неизвестна: нефротоксичность (например, почечная недостаточность,
интерстициальный нефрит, нефротический синдром, повышение уровней
мочевины или креатинина в крови).
Нарушения
со стороны репродуктивной системы и молочной железы
Сообщалось
об отдельных случаях женского бесплодия при лечении препаратами,
подавляющими синтез циклооксигеназы/простагландинов, включая
теноксикам.
Противопоказания
—
повышенная чувствительность к компонентам препарата,
ацетилсалициловой кислоте или другим НПВП
—
повышенная
чувствительность
(включая симптомы астмы, ринит, ангионевротический отек или
крапивницу) к салицилатам, ибупрофену, аспирину или другим НПВС
—
активные
или имеющиеся в анамнезе рецидивирующие пептическая язва/кровотечение
(два или более явных случаев доказанного изъязвления или
кровотечения);
—
желудочно-кишечное
кровотечение (мелена, кровавая рвота), перфорация, вызванная
предыдущим применением НПВС, или тяжелый гастрит в анамнезе
—
выраженные нарушения функции печени и почек
—
сахарный диабет
—
артериальная гипертензия, сердечная недостаточность, отеки
—
беременность, период лактации
—
лицам с наследственной непереносимостью фруктозы, дефицитом фермента
Lapp-лактазы,
мальабсорбцией глюкозы-галактозы
—
детский возраст до 18 лет.
Лекарственные взаимодействия
Другие
анальгетики, включая селективные ингибиторы циклооксигеназы-2
Следует
избегать одновременного применения двух или более НПВС (включая
аспирин), так как при этом может повышаться риск возникновении
неблагоприятных эффектов.
Ацетилсалицилаты
и салицилаты
Салицилаты
способны вытеснять теноксикам из мест связывания с белками, таким
образом повышая клиренс и объем распределения препарата Артоксан. По
этой причине следует избегать одновременного применения салицилатов,
так как при этом повышается риск возникновения неблагоприятных
реакций (в частности, желудочно-кишечных).
Антациды
и антагонисты рецепторов H2
Антациды
могут снижать скорость абсорбции препарата Артоксан, но не ее
степень. Разница не является клинически значимой. Не наблюдалось
взаимодействия с принимаемым одновременно циметидином.
Антикоагулянты
Теноксикам
в значительной степени связывается с альбумином сыворотки крови и,
как и все НПВС, усиливает эффекты антикоагулянтов, таких как
варфарин. Рекомендуется тщательно контролировать эффекты
антикоагулянтов и пероральных гликемических средств, в особенности на
начальных этапах лечения препаратом Артоксан. Не наблюдалось
взаимодействия с дигоксином. У здоровых субъектов не отмечалось
клинически значимого взаимодействия между препаратом Артоксан и
гепарином с низкой молекулярной массой.
Сердечные
гликозиды
НПВС
могут обострять сердечную недостаточность, снижать скорость
клубочковой фильтрации и повышать уровни сердечных гликозидов в
плазме крови при одновременном применении с сердечными гликозидами.
Циклоспорин
Как
и в случае с другими НПВС, рекомендуется соблюдать осторожность при
одновременном применении циклоспорина по причине повышенного риска
нефротоксичности.
Хинолоновые
антибиотики
Результаты
исследований на животных показывают, что НПВС способны повышать риск
возникновения судорог, вызванных хинолоновыми антибиотиками.
Пациенты, принимающие НПВС и хинолоны, могут иметь повышенный риск
развития судорог.
Литий
Нестероидные
противовоспалительные средства снижали выведение лития. При
назначении теноксикама пациенту, принимающему литий, необходимо
увеличить частоту мониторинга уровней лития и предупредить пациента о
необходимости потребления достаточного количества жидкости и о
симптомах интоксикации литием.
Диуретики
и антигипертензивные средства
Нестероидные
противовоспалительные средства способны вызывать задержку натрия,
калия и жидкости и препятствовать натрийуретическому действию
диуретиков, что может привести к повышению риска нефротоксичности
НПВС. Необходимо помнить о данных особенностях при лечении пациентов
с нарушением функции сердца или гипертензией, так как они могут быть
восприимчивыми к ухудшению данных состояний.
Не
наблюдалось клинически значимого взаимодействия между препаратом
Артоксан и фуросемидом, однако препарат Тилкотил ослабляет эффект
снижения кровяного давления, вызванный гидрохлортиазидом. Как
известно из информации о других НПВС, препарат Артоксан может
ослаблять антигипертензивный эффект альфа-адренергических блокаторов
и ингибиторов АПФ.
Не
сообщалось о взаимодействии между препаратом Артоксан и
альфа-агонистами центрального действия или блокаторами кальциевых
каналов.
Не
отмечалось клинически значимого взаимодействия при одновременном
применении препарата Артоксан с атенололом. Во время клинических
исследований не наблюдалось взаимодействия у пациентов, одновременно
принимавших препараты наперстянки. Таким образом, не ожидается
значительного риска при одновременном применении препарата Артоксан и
дигоксина.
Метотрексат
Рекомендуется
соблюдать осторожность при одновременном применении метотрексата по
причине возможного усиления его токсичности, так как сообщалось о
снижении выведения метотрексата под действием НПВС.
Пероральные
противодиабетические средства
Клинический
эффект пероральных противодиабетических средств глиборнурида,
глибенкламида, толбутамида не изменялся под действием препарата
Артоксан. Тем не менее, как и в случае с другими НПВС, рекомендуется
проводить тщательный контроль пациентов, одновременно принимающих
пероральные противодиабетические средства.
Колестирамин
Колестирамин
может усиливать выведение и сокращать период полувыведения
теноксикама.
Декстрометорфан
Одновременное
применение теноксикама и декстрометорфана может усиливать
анальгетический эффект по сравнению с монотерапией.
Пища
Степень
абсорбции теноксикама не изменяется при одновременном приеме пищи, но
скорость абсорбции (Cmax)
может быть более медленной, чем в состоянии натощак.
Иное
Одновременное
применение пробенецида и теноксикама может повышать концентрацию
теноксикама в плазме крови. Клиническая значимость данного наблюдения
не установлена.
Мифепристон
Не
следует принимать НПВС в течение 8-12 дней после применения
мифепристона, так как НПВС могут снижать эффект мифепристона.
Кортикостероиды
Как
и в случае со всеми другими НПВС, необходимо соблюдать осторожность
при одновременном применении кортикостероидов по причине повышенного
риска возникновения желудочно-кишечной язвы или кровотечения.
Антитромбоцитарные
средства и селективные ингибиторы обратного захвата серотонина
(СИОЗС)
Риск
возникновения желудочно-кишечного кровотечения повышается при
одновременном применении антитромбоцитарных средств и селективных
ингибиторов обратного захвата серотонина (СИОЗС) с НПВС.
Такролимус
Риск
нефротоксичности повышается при применении НПВС с такролимусом.
Зидовудин
Риск
гематологической токсичности увеличивается при применении НПВС вместе
с зидовудином. Имеются свидетельства повышения риска возникновения
гемартроза и гематом у ВИЧ-положительных пациентов с гемофилией,
одновременно принимающих зидовудин и ибупрофен.
Особые указания
Желудочно-кишечное
кровотечение, язва и перфорация
ЖК
кровотечение, язва или перфорация, которые могут иметь летальный
исход, наблюдались при применении всех НПВС в любой момент курса
лечения при наличии или отсутствии предупреждающих симптомов или
серьезных ЖК явлений в анамнезе.
Риск
возникновения ЖК кровотечения, язвы или перфорации повышается при
увеличении дозы НПВС, а также у пациентов с язвой в анамнезе, в
особенности с язвой, осложненной кровотечением или перфорацией и у
пожилых пациентов. Таким пациентам следует начинать лечение с
минимальной возможной дозы. Необходимо рассмотреть возможность
комбинированного лечения защитными средствами (например,
мизопростолом или ингибиторами протонного насоса) у таких пациентов,
а также у пациентов, которым требуется применение низких доз аспирина
или иных препаратов, способных повышать желудочно-кишечный риск.
Пациенты
с ЖК токсичностью в анамнезе, в частности, пожилые пациенты, должны
сообщать обо всех необычных симптомах со стороны живота (в
особенности о ЖК кровотечениях), особенно в начале лечения.
Следует
соблюдать осторожность при лечении пациентов, одновременно
принимающих препараты, способные повышать риск изъязвления или
кровотечения, такие как пероральные кортикостероиды, антикоагулянты,
например, варфарин, селективные ингибиторы обратного захвата
серотонина или антитромбоцитарные средства, такие как аспирин.
При
возникновении ЖК кровотечения или язвы у пациентов, принимающих
теноксикам, необходимо прекратить лечение.
Следует
соблюдать осторожность при применении НПВС у пациентов с
желудочно-кишечными заболеваниями (язвенным колитом, болезнью Крона)
в анамнезе, так как подобные состояния могут обостряться.
Нарушения
со стороны дыхательной системы
Необходимо
соблюдать осторожность при лечении пациентов с имеющейся или
указанной в анамнезе бронхиальной астмой, так как ибупрофен вызывал
бронхоспазм у таких пациентов.
Сердечно-сосудистые
и цереброваскулярные эффекты
Соответствующий
мониторинг и консультации необходимы пациентам с гипертензией и/или
умеренной застойной сердечной недостаточностью в анамнезе, так как
сообщалось о задержке жидкости и отеке при лечении НПВС.
Результаты
клинических и эпидемиологических исследований показывают, что
применение некоторых НПВС (в особенности в высоких дозах и при
продолжительном лечении) может вызывать небольшое повышение риска
артериальных тромботических явлений (например, инфаркта миокарда или
инсульта). Данные являются недостаточными для исключения подобного
риска для теноксикама.
Пациенты
с неконтролируемой гипертензией, застойной сердечной
недостаточностью, установленной ишемической болезнью сердца,
заболеванием периферических артерий и/или цереброваскулярным
заболеванием могут подвергаться лечению теноксикамом только после
тщательной оценки. Аналогичная оценка требуется перед началом
долгосрочного лечения пациентов с факторами риска
сердечно-сосудистого заболевания (например, гипертензией,
гиперлипидемией, сахарным диабетом, курением).
Препарат
Артоксан содержит лактозу.
Пациентам
с редкими наследственными проблемами непереносимости галактозы,
лактазной недостаточностью Лаппа или мальабсорбцией глюкозы-галактозы
не следует принимать данный препарат.
Применение
в педиатрии
Препарат
противопоказан к применению у детей и подростков до 18 лет (в виду
недостаточности клинических данных).
Беременность
и лактация
Препарат
противопоказан к применению в период беременности и в период
лактации.
Теноксикам
и его метаболиты проникают в грудное молоко, поэтому препарат не
рекомендуется применять в период грудного вскармливания.
Особенности
влияния лекарственного средства на способность управлять транспортным
средством или потенциально опасными механизмами
В
период лечения необходимо воздерживаться от занятий потенциально
опасными видами деятельности, требующими повышенной концентрации
внимания и быстроты психомоторных реакций.
Передозировка
Симптомы:
отмечается
усиление побочных эффектов.
Лечение:
специфического антидота не существует. При подозрении на
передозировку теноксикама рекомендуется симптоматическая терапия.
Форма выпуска и упаковка
По
10 таблеток в контурной ячейковой упаковке из пленки
поливинилхлоридной и фольги алюминиевой.
По
1 контурной ячейковой упаковке вместе с инструкцией по медицинскому
применению на государственном и русском языках помещают в картонную
коробку.
Условия хранения
Хранить
при температуре не выше 25°С.
Хранить
в недоступном для детей месте!
Срок хранения
3
года
Не
применять по истечении срока годности.
Условия отпуска из аптек
По
рецепту
Производитель/Упаковщик
«Уорлд
Медицин Илач Сан. ве Тидж. А.Ш.», Турция
(Багджылар
Илчеси, Гюнешли, Эврен Махаллеси, Джами Йолу Джад. №50
К.
1В
Земин
4-5-6, Стамбул)
“World
Medicine İlaç San. ve Tic. А.Ş.”,
Turkey
(Bağcılar
İlçesi, Güneşli, Evren Mahallesi, Cami Yolu
Cad. No:50 K. 1B Zemin 4-5-6, İstanbul).
Владелец регистрационного удостоверения
«РОТАФАРМ
ИЛАЧЛАРЫ ЛИМИТЕД ШИРКЕТИ», ТУРЦИЯ
Адрес
организации, принимающей на территории Республики Казахстан претензии
от потребителей по качеству продукции
РК,
Алматы, ТОО «TROKA—S
PHARMA»,
пр.Суюнбая, 222 Б
Тел/факс:
8 (7272) 529090
Адрес
организации ответственной за пострегистрационное наблюдение за
безопасностью лекарственного средства:
ТОО
«TROKA—S
PHARMA»,
РК, г. Алматы, пр. Суюнбая, 222 Б
Сотовый
тел +7 701 786 33 98, (24-часовой доступ).
е-mail:
pvpharma@worldmedicine.kz
| Артоксан,_таблетки_(каз.)_.doc | 0.1 кб |
| Артоксан,_таблетки_(рус).doc | 0.08 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Способ применения и дозировка
Внутрь, в одно и тоже время суток, запивая водой или другой жидкостью, в дозе 20 мг 1 раз в сутки; поддерживающая доза — 10 мг/сут. При острых приступах подагры — по 40 мг 1 раз в сутки в течение первых 2-х дней, затем — 20 мг 1 раз в сутки в течение 5 дней. Пациентам пожилого возраста назначают в дозе 20 мг/сут.
Условия хранения
Список Б. В сухом защищенном от света месте при комнатной температуре.
Состав
Действующее вещество — Теноксикам.
Передозировка
Данных нет.
Особые указания
С осторожностью используют для лечения пожилых, на фоне диуретиков, нефротоксических препаратов, непосредственно после хирургических вмешательств. За несколько дней до хирургического вмешательства теноксикам следует отменить. В процессе длительного лечения необходим контроль функции печени и почек, протромбинового индекса, глюкозы в крови. Развитие на фоне лечения эрозивно-язвенного поражения или кровотечения из ЖКТ требует отмены препарата и назначение соответствующей терапии.
При применении с диуретиками и больным с артериальной гипертензией и сердечной недостаточностью следует учитывать возможность задержки натрия и воды в организме.
Взаимодействие
Усиливает эффект препаратов лития (в т.ч. токсичность), непрямых антикоагулянтов, пероральных гипогликемизирующих средств (производные сульфанилмочевины). Антациды снижают скорость всасывания. Другие НПВС повышают риск развития побочных проявлений, особенно со стороны ЖКТ.
Фармакологическое действие
Противовоспалительное, жаропонижающее, анальгезирующее. Противовоспалительный эффект обусловлен уменьшением проницаемости капилляров (ограничивает экссудацию), стабилизацией лизосомальных мембран (препятствует выходу ферментов лизосом, вызывающих повреждение тканей), торможением выработки макроэргов, в т.ч. АТФ, угнетением синтеза или инактивацией медиаторов воспаления (ПГ, гистамина, брадикинина, лимфокинов, факторов комлемента). Уменьшает количество свободных радикалов в очаге воспаления, угнетает хемотаксис и фагоцитоз. Снижает болевую чувствительность в очаге воспаления и действует на таламические центры боли. Оказывает десенсибилизирующее действие (при длительном применении).
Быстро и полностью всасывается в ЖКТ; прием пищи замедляет скорость абсорбции. Биодоступность полная. Легко проходит через гистогематические барьеры. Основная часть выводится в виде неактивных метаболитов с мочой, остальная — с желчью.
При ревматических заболеваниях ослабляет боль в суставах в покое и при движении, уменьшает утреннюю скованность и припухлость суставов, улучшает функции и увеличивает объем движений суставов. Противовоспалительный эффект развивается к концу первой недели лечения.
Показания к применению
Воспалительно-дегенеративные заболевания опорно-двигательного аппарата, сопровождающиеся болевым синдромом: суставной синдром при подагре, ревматоидный артрит, остеоартроз, анкилозирующий спондилит, остеохондроз, суставной ревматизм (тендиниты, бурситы, миозиты); боль в позвоночнике, невралгия, миалгия, травмы.
Побочное действие
Тошнота, изжога, боли и неприятные ощущения в животе, диарея, метеоризм, стоматит, анорексия, эрозивно-язвенные поражения, кровотечения, перфорация, головная боль, головокружение, бессонница, депрессия, повышенная возбудимость, отек или раздражение глаз, нарушения зрения, периферические отеки, повышение концентрации в плазме креатинина, мочевины азота, билирубина и активности печеночных трансаминаз, удлинение времени кровотечения, аллергические реакции в виде крапивницы, зуда, эритемы, синдрома Стивенса-Джонсона и Лайелла. При применении свечей возможно местное раздражение, болезненная дефракция.
Противопоказания
Гиперчувствительность, эрозивно-язвенные поражения ЖКТ (в т.ч. в анамнезе), желудочно-кишечное кровотечение (в т.ч. в анамнезе), гастрит тяжелого течения, «аспириновая» триада, выраженные нарушения функции печени и почек, почечная недостаточность, сахарный диабет, артериальная гипертензия, сердечная недостаточность, беременность, кормление грудью (на время лечения прекращают), детский возраст.
